没收到验证邮件?请确认邮箱是否正确或 重新发送邮件

#本文仅代表作者观点,不代表IPRdaily立场#
来源:IPRdaily中文网(iprdaily.cn)
原标题:最新!阿布昔替尼在中国获批上市,大为发布专利全景报告纵览全球布局
FDA新批准药物一直是国内药企进行新药研发的重要风向标,对FDA每月新批准的药品尤其是NME(新分子实体)的专利保护情况进行剖析,可以帮助国内企业尽早了解专利壁垒,确定研发方向。
据世界卫生组织(WHO)数据显示,全球至少2.5亿人受到特应性皮炎(Atopic dermatitis,简称“AD”)疾病困扰,中国AD症的发病率呈现逐年递增趋势且总病患人数已经超过7000万。著名分析机构Global Data预测AD药物市场将以11.1%的年复合增长率在2027年突破170亿美元,辉瑞、赛诺菲、艾伯维等制药巨头纷纷布局该赛道并推动了靶向生物制剂和小分子抑制剂陆续进入市场。
美国FDA于2022年1月14日批准辉瑞公司的NME药品阿布昔替尼上市,该药物用于治疗特应性皮炎(Atopic dermatitis,简称“AD”)。国家药品监督管理局(NMPA)于4月11日公布已批准辉瑞公司的阿布昔替尼片在中国上市。作为辉瑞力推的重磅创新药物,阿布昔替尼未来有望打破AD药物市场度普利尤单抗一枝独秀的局面。
本文通过对该药品的全球审批信息和全球专利布局情报全面收集和多维度解读,为国内药企在阿布昔替尼上的研发决策提供支撑;通过对阿布昔替尼核心专利保护范围的层层剖析和技术内容的深度解析,为国内药企寻找技术突破点、提升研发效率助力。
1、阿布昔替尼在全球申报/上市情况
2022年1月14日,美国FDA批准辉瑞公司CIBINQO®(中文商品名希必可®,英文通用名称Abrocitinib,中文通用名称阿布昔替尼,剂量是50mg、100mg、200mg)用于治疗中重度AD症成人患者,作为新化学实体NCE,阿布昔替尼同时获得了5年的市场独占权,保护期限至2027年1月14日,这就意味着FDA在2027年前不会批准任何ANDA申请(仿制药的简化新药申请)。
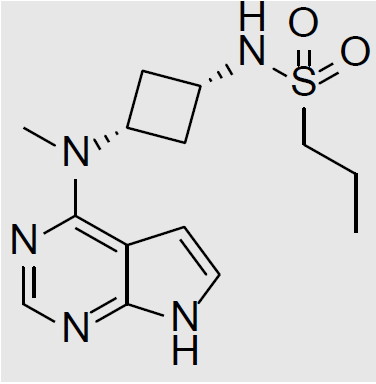
阿布昔替尼化学结构式[1]
CIBINQO®已于2021年9月起先后被英国MHRA(9月12日)、日本MHLW(9月30日)、欧盟EMA(12月16日)批准;中国NMPA于2022年4月11公布通过优先审评审批程序批准辉瑞公司申报的1类创新药阿布昔替尼片(商品名:希必可®/CIBINQO®)上市,该药适用于对其他系统治疗(如激素或生物制剂)应答不佳或不适宜上述治疗的难治性、中重度特应性皮炎成人患者。
2、阿布昔替尼专利布局情况
通过对当前全球已公开的105条阿布昔替尼专利进行阅读整理,并按照专利申请人、专利申请时间、专利布局类型、布局区域、重点区域保护等进行梳理,绘制成如下图所示的专利布局全景图。为方便梳理技术脉络,仅分析简单同族合并后的6项WO同族专利(由于药物的特殊性和普适性,医药企业普遍重视专利的海外地域布局,通过PCT途径就同一技术方案在全球多个国家或地区进行布局是经常选用的最重要的方式,故进行简单同族专利合并时优先保留WO专利申请)。

图1 阿布昔替尼专利布局全景图
在阿布昔替尼的6项专利中,有4项来自于原创药厂家辉瑞公司,辉瑞公司早在药品上市前7年已经开始就阿布昔替尼进行专利布局,其专利申请大体上遵循“早期发现阶段申请基础化合物专利、相近母核结构的衍生物专利,开发阶段申请活性化合物的晶型或盐的专利、新中间体及制备方法专利,临床阶段申请药物组合物、新晶型”的策略。
另外2项专利来自其他医药企业申请的外围晶型专利。由于晶型会影响药物的稳定性、生物利用度及疗效,故晶型专利是在药物上市前后被医药企业纷纷抢占的专利申请热点,涉及单体、溶剂化物、盐和水合物等各种形式的多晶型。
2.1 基础化合物专利布局
阿布昔替尼的基础化合物专利来自于原创药厂家辉瑞公司,辉瑞公司在2013年2月22日提交了关于阿布昔替尼马库什结构化合物的临时专利申请No.61/767947(专利名称为Pyrrolo[2,3-D]Pyrimidine Derivatives),并在12个月优先权期限内先向WIPO国际局提交了PCT申请PCT/IB2014/058889以期在较短的时间内可以进入尽可能多的国家和地区,该专利申请的公开号是WO2014128591A1,申请日2014年2月11日;后于2014年2月19日向美国专利商标局提交了正式申请14/183,946(专利公开号是US20140243312A1,授权公告号是US9035074B2)。作为仿制药企业无法规避的最重要专利,辉瑞公司就该专利的技术内容在全球53个国家或地区申请了72件简单同族专利,保护地域包括美国、中国、丹麦、塞浦路斯、西班牙、匈牙利、德国、加拿大、欧洲、韩国、日本、澳大利亚等。
鉴于阿布昔替尼在美国、日本、欧洲已经上市,在中国也即将上市,故选定中国、美国、日本和欧洲作为重点区域,通过梳理专利在重点区域的同族专利分布,了解仿制药在这些区域的最早进入时机。
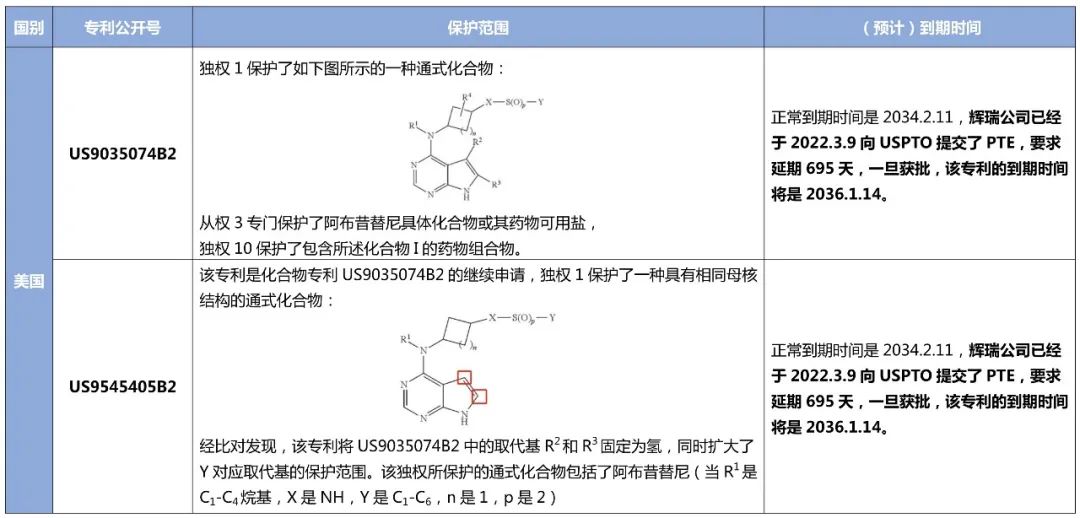
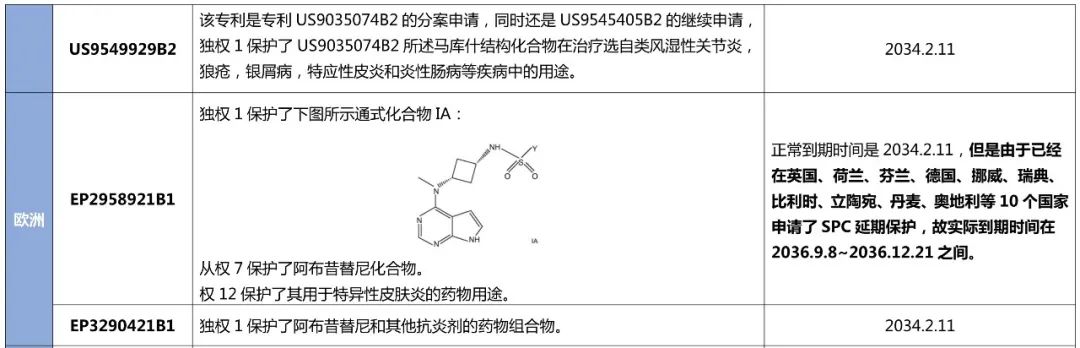
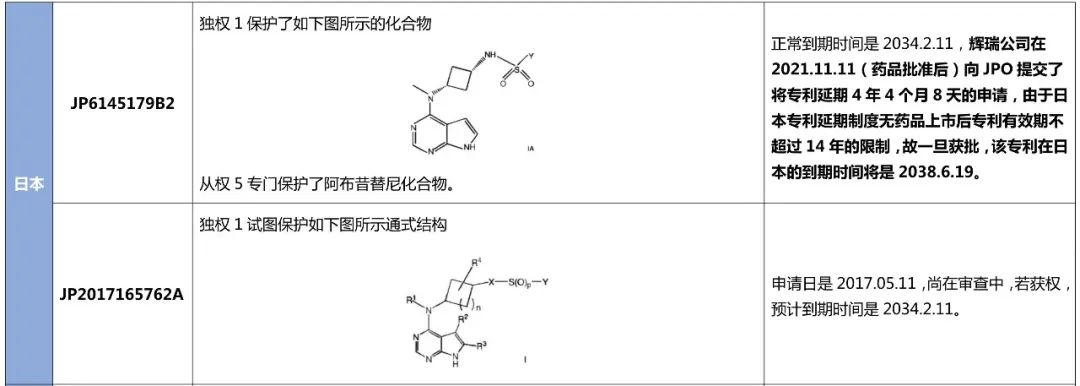
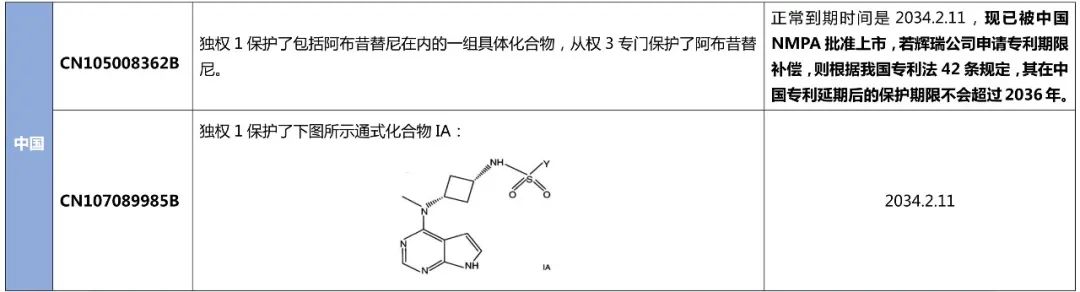
WO2014128591A1在美国共有三件同族专利,分别是US9035074B2、US9545405B2和US9549929B2,均已授权且被列入Orange Book(橙皮书)中,辉瑞已就前两件专利于2022年3月9日向USPTO提交了延期保护申请。在欧洲的同族专利EP2958921B1和EP3290421B1已经获得授权,且前者还获得SPC延期;在日本的同族专利,分别是JP6145179B2和JP2017165762A,前者已经获得授权且申请了专利延期保护;在中国也有两件同族专利,分别是CN105008362B和CN107089985B,上述专利的保护范围和(预计)到期时间详情见下表。
表 1 阿布昔替尼基础化合物专利在重点区域的保护情况
2.2 衍生物专利布局
辉瑞公司于2014年8月12日申请了阿布昔替尼相似结构衍生物的专利(结构式如下所示)WO2016024185A1。
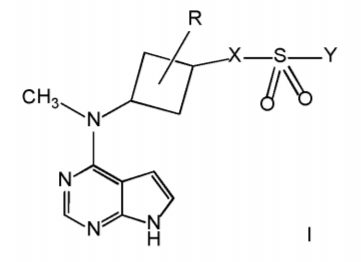
与WO2014128591A1中试图保护的阿布昔替尼通式化合物的结构相比,本专利申请的不同点在于将R1固定为甲基,R2、R3固定为氢,四元环数量n固定为1,氧原子数量p固定为2,并对Y取代基可能包含的基团范围进行了扩展。辉瑞公司通过对化合物衍生物的保护,试图对该类化合物做到最大范围的保护。
该申请目前已进入美国、日本、韩国、加拿大、乌拉圭等8个国家或地区,但并未进入中国,故该专利中公开的化合物可以供国内采用Fast Follow的药企做药物研究参考。
2.3 药物新用途专利
辉瑞公司于2020年9月8日申请了阿布昔替尼用于治疗汗腺炎的新用途专利WO2021048736A1,该专利的优先权日是2019年9月11日,当前仅进入了阿根廷、日本和台湾,由于该国际申请尚未超出进入国家阶段的最晚期限(2022年5月11日),故依然有进入中国的可能性。
2.4 药物晶型专利
当前已公开的阿布昔替尼晶型专利共有3件,2019年辉瑞公司先申请了一件晶型专利WO2020008391A1,自2020年起其他医药企业陆续开始就阿布昔替尼申请外围专利,当前已有印度的格伦马克生命科学公司和苏州晶云药物科技公司先后申请了阿布昔替尼的晶型专利WO2020261041A1和WO2021218948A1。
2.4.1 辉瑞公司关于阿布昔替尼的晶型专利
在阿布昔替尼进入临床研究后,辉瑞公司开始提交该化合物的中间体和晶型专利,以期在对其进行全方位保护的同时延长药品的专利生命周期。
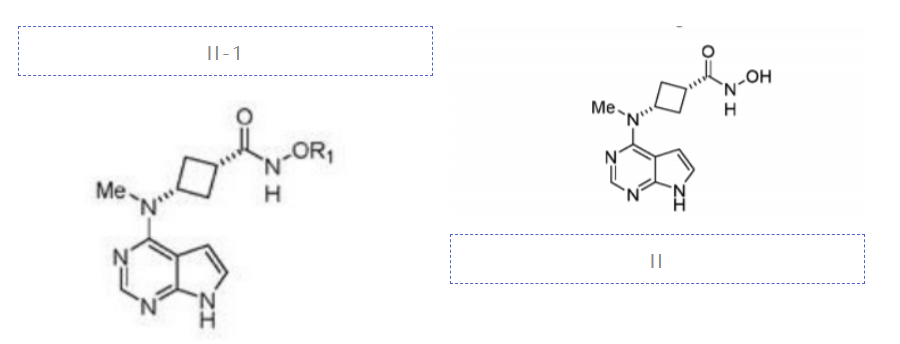
WO2020008391A1申请日是2019年5月31日,其权利要求书除了试图保护具有上述结构的中间体(II)、由该中间体制备阿布昔替尼的工及由此工艺得到的阿布昔替尼的晶型I(XRPD图θ峰在13.0°、14.8°和23.3°±0.2° 2θ处),还试图保护阿布昔替尼的酸式盐,从国际初步审查报告来看,上述拟保护范围均有新颖性,但阿布昔替尼酸式盐的创造性不足。该申请目前已进入中国、美国、日本、韩国、欧洲、加拿大、澳大利亚等13个国家或地区。
2.4.2 格伦马克生命科学公司关于阿布昔替尼的新晶型专利
印度的仿制药企业格伦马克生命科学公司(Glenmark Life Sciences Limited)在2020年6月16日提交了关于阿布昔替尼新晶型制备工艺的专利WO2020261041A1,其权利要求书除了试图保护制备晶体阿布昔替尼(XRPD图的θ峰在12.9°、14.7°、19.4°、23.2° 和 25.2 ±0.2°2θ处)的方法外,还试图保护阿布昔替尼的无定形固体分散体。
格伦马克生命科学的专利申请策略是2019年6月27日先在本国申请专利(IN201921025659A),然后于12个月优先权内提交PCT申请(WO2020261041A1),目前该PCT申请仅进入了欧洲(尚未公开),并未进入中国,由于其进入中国国家阶段的最晚期限是2022年2月27日,故该专利申请不会再有中国同族。做阿布昔替尼晶型研究的国内企业可以参考该专利中公开的晶型表征数据。
2.4.3 苏州晶云药物科技公司关于阿布昔替尼的晶型专利
作为首家专注于药物晶型研发和产业化的中国公司,苏州晶云药物科技股份有限公司在其国内申请CN202010347086.0(公开号CN113637018A,申请日是2020年4月27日))的基础上,于2021年4月27日提交了关于阿布昔替尼新晶型B、C、D、E、F的PCT申请WO2021218948A1,目前该PCT申请仅进入了欧洲(尚未公开),从受理局提供的国际检索报告来看,部分晶型并不具备新颖性。
3、技术研发时机和专利布局启示
3.1 市场规模可观,可考虑进入该领域
全球高达10%的成人和20%的儿童(至少2.5亿人)受到AD疾病困扰,亟需有效治疗方法来缓解症状,阿布西替尼市场规模预计将在2027年突破170亿美元,可见阿布昔替尼市场前景乐观,可考虑进入该领域。但也要持续关注市场表现,动态调整研发策略。
3.2 不同类型企业应选择合适的时机及研发切入点进入
辉瑞公司通过基础化合物专利WO2014128591A1和衍生物专利WO2016024185A1试图对如下图所示的马库什结构的化合物做到最大程度的保护:
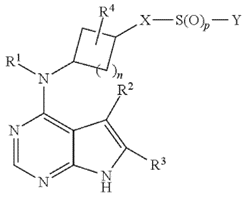
且辉瑞公司目前仅有一件晶型专利WO2020008391A1,其试图保护一种新的中间体和由该新中间体制备阿布昔替尼晶体的方法,但是并未试图保护该晶型,从专利说明书公开内容可以推断出专利中所述晶型I因已经被基础化合物专利的制备工艺所公开而丧失了新颖性,同时当前上市的阿布昔替尼口服片也是晶型I。
因此对于国内不同类型药企来讲,研发时机和技术切入点有所不同。
Fast Follow医药企业:分析基础化合物专利的保护范围,参考阿布昔替尼二期临床实验以来的所有相似结构化合物,判断取代基可能存在的突破点在哪里,进而研究Me-too或Me-better药物。
仿制药企业:由于其基础化合物专利在中国、美国、日本和欧洲等重点区域的到期时间不会早于2036年,故可结合自身优势尽快立项研发,并积极对辉瑞公司的基础化合物专利在中国的同族专利CN105008362B进行稳定性评估判断专利(部分)无效的可能性。
CDMO企业:跟踪原创药产品管线进展,并在中间体或晶型研究上创新,像苏州晶云科技,因其突出的晶型研发能力,极有可能成为辉瑞公司就阿布昔替尼剂型改进的合作伙伴。
原料药供应企业:可参照辉瑞公司基础化合物专利中的制备工艺进行产品研发,使得制备的阿布昔替尼原料药除了基础化合物外不会侵犯其他在后外围专利,如用不同于WO2020008391A1中所公开的晶型I的制备方法制备晶型I,应该不会落入该专利的保护范围(但依然落入基础化合物专利的保护范围)。从而确保产品尽早供给市场。
3.3 进入该领域的企业,专利布局和侵权风险排查应一并开展
从阿布昔替尼的专利布局全景图来看,当前辉瑞公司虽然已经申请了基础化合物专利、衍生物专利、晶型专利等4项专利,但是专利数量(指简单同族合并后的数量)、专利类型丰富度和专利保护范围的多维性尚不足,这对国内企业研发阿布昔替尼无疑是一大利好。
未来几年围绕阿布昔替尼的外围专利数量会出现明显增加,专利申请的热点除了晶型专利外,还会在组合物专利、新中间体和制备工艺上。国内企业既要对研发成果积极通过申请专利进行保护,也当持续跟踪辉瑞公司的专利布局动态,做好专利防侵权评估。
数据说明
为全面获取阿布昔替尼的全球专利数据,本报告以阿布昔替尼的中英文名称、商品名、实验室代码、化学名称、CAS号、结构式等作为检索要素,选用美国食品药品监督局FDA网站、SciFinder Scholar、药渡数据和innojoy专利数据库等四个平台分别制定不同的检索策略,共获得原始专利数据206条,经过人工阅读筛选和简单同族专利合并,最终得到与阿布昔替尼相关的专利105条(检索截止日2022年3月22日)。
附:完整版《阿布昔替尼专利分析报告》目录

立即扫码获取完整版《阿布昔替尼专利分析报告》

欲咨询、交流或索取报告,可扫码加入医药粉丝群

基于本报告,大为将于4月21日19:00进行【专利分析助力药品研发与布局】的主题直播,欢迎大家扫码报名。

直播大纲
一、医药创新离不开专利分析
1.医药行业高投入、高风险、高回报
2.药品对于专利的依赖度高
二、如何做药品专利布局分析
1.全球审批信息收集
2.全面、准确的专利检索
3.专业、详实的专利分析
三、阿布西替尼专利布局案例分享
1.阿布西替尼全球审批信息速递
2.阿布西替尼全球专利布局分析
3.技术研发及专利布局启示
*本文为大为咨询团队原创,文章内容文字、图片和音视频资料,版权均属大为知识产权所有,任何媒体、网站或个人未经授权不得转载、链接、转贴或以其他方式复制发布/发表。已获授权的媒体、网站或个人使用时请注明"稿件来源:大为知识产权",商业使用请联系:18531281151。
注释
[1]化学结构式来自于FDA上提供的阿布昔替尼的LABEL information。
来源:IPRdaily中文网(iprdaily.cn)
编辑:IPRdaily王颖 校对:IPRdaily纵横君
注:原文链接:最新!阿布昔替尼在中国获批上市,大为发布专利全景报告纵览全球(点击标题查看原文)
与光同行!2021年中国“40位40岁以下企业知识产权精英”榜单揭晓
两天掌握涉外商标代理业务!涉外商标代理高级研修班「北京站」来啦

「关于IPRdaily」
IPRdaily是全球领先的知识产权综合信息服务提供商,致力于连接全球知识产权与科技创新人才。汇聚了来自于中国、美国、欧洲、俄罗斯、以色列、澳大利亚、新加坡、日本、韩国等15个国家和地区的高科技公司及成长型科技企业的管理者及科技研发或知识产权负责人,还有来自政府、律师及代理事务所、研发或服务机构的全球近100万用户(国内70余万+海外近30万),2019年全年全网页面浏览量已经突破过亿次传播。
(英文官网:iprdaily.com 中文官网:iprdaily.cn)
本文来自IPRdaily中文网(iprdaily.cn)并经IPRdaily.cn中文网编辑。转载此文章须经权利人同意,并附上出处与作者信息。文章不代表IPRdaily.cn立场,如若转载,请注明出处:“http://www.iprdaily.cn

 共发表文章1873篇
共发表文章1873篇文章不错,犒劳下辛苦的作者吧
- 我也说两句
- 还可以输入140个字














